全国の基幹的医療機関に配置されている『ロハス・メディカル』の発行元が、
その経験と人的ネットワークを生かし、科学的根拠のある健康情報を厳選してお届けするサイトです。
情報は大きく8つのカテゴリーに分類され、右上のカテゴリーボタンから、それぞれのページへ移動できます。
アルツハイマー病の25%、実は違う病気だった?
臨床的に診断されたアルツハイマー病の25%が、実際にはアルツハイマー病ではなく、神経細胞の老化によって起きる「高齢者タウオパチー」などの別の病気であることが報告されているという。11月21日に京大が開いた記者セミナーで医学部人間健康科学科の木下彩栄教授が解説した。
ロハス・メディカル論説委員 熊田梨恵
巷では認知症と言えばアルツハイマー病という雰囲気があるが、研究が進むことで、神経細胞の老化によって引き起こされている別の病気も含まれていることが分かってきた、という話だ。一般向けにはあまり伝えられていないと思うので書いておく。しかしこうなると、そもそも老化そのものを防げるのかという別の話になってきそうな気もした。
木下教授の記者セミナーでの話を基に書く。(掲載しているスライドは全てセミナー時に配られた木下教授作成のもの。黒い汚れのようなものは筆者のメモの残り)
==================
この話の予備知識として、まず現在アルツハイマー病がどのように診断されているかを知る必要がある。
アルツハイマー病は、
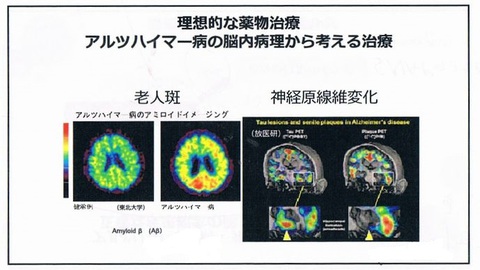
①アミロイドβと呼ばれるたんぱく質(老人斑)がたまっていること
②リン酸化されたTau(タウ)たんぱく質が神経細胞の中にたまって神経細胞を殺してしまうこと(神経原線維変化)
この2つの状態によって起こるとされる。
(「認知症を知る2 アルツハイマー型」ロハス・メディカル2012年7月号参照)
つまり、脳の中にこの2つの物質を確認しないといけないわけだが、これまではそのバイオマーカーが見つかっていなかった。脳を取り出してこれらのタンパク質があるか否かと見るわけにもいかないので、実際の診断は一般的に以下のように行われている。
<アルツハイマー病と診断されるまでの大まかな流れ>(順序は異なることあり。別の検査が行われることもある)
一般的な身体検査
↓
知的機能の測定テスト(臨床的に記憶障害があるか否かを見る)
↓
脳の検査、画像診断検査(MRIなど海馬の萎縮を見る)
↓
専門医がこれらを総合的に診て診断
==================
しかし現在では技術が進み、「アミロイドPET」という医療機器(約3年前に日本で開発)によってアミロイドβが可視化できるようになってきた。海馬周辺に神経原線維変化がTauという形でたまってきているということが分かるようになった。スライドの左側がアミロイドPET、左側がTauPETによるもの。
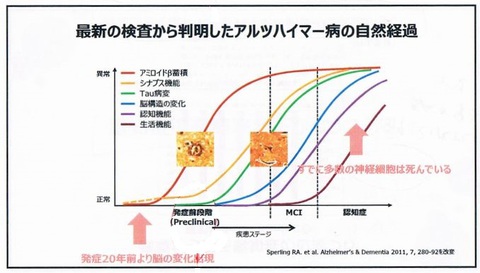
最近の検査から判明したアルツハイマー病の自然経過について、木下教授の説明。
・すでにプレクリニカルの状態で老人斑がぐっと溜まっているのが分かる。MCI(軽度認知症)の時には既にピークに達していて、認知症になっても変わらない。
・これに神経原線維変化が誘発されて上がってくる。
・最終的に脳構造の変化、海馬の萎縮が起きて、認知機能が低下して、生活障害が見られる。
・これまで認知症は歳を取って発症すると思われていたが、違う。アルツハイマー病というのは、発症する20年以上前から脳に変化が出現している病気ということが明らかになった。発症してからでは治療しても遅い。神経細胞の中に既に神経原線維変化がたくさんたまっており、取り除くのは不可能。これまでは発症後をターゲットとしていたが、もう遅い。
・理想的には老人斑がたまらない状態になっていれば神経は死なないのでは、と考えられていて、今はできるだけ早期に治療を開始するのが良いと考えられている。
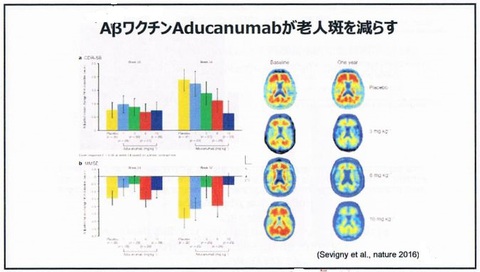
・一例として、老人斑を消す「Aβワクチン」というワクチンが複数開発されている。アミロイドβに対して注射するもの。
・あまりうまくいっていないが、唯一上手くいっている例が去年9月にNATUREに出たこの報告。ワクチンの量をどんどん増やして打っていき、1年後のアミロイドβ量を見る。ワクチン量が増えるに従い、アミロイドβ量は減っていることが分かる。実際に認知機能も改善した。これは非常にマイルドな早期のアルツハイマー病の患者で起きたこと。
・ここから考えられることは、アルツハイマー病は発症してからの治療では限界があるということ。アルツハイマー病の症状が出る随分前、物忘れの症状が出る前ぐらいからやっておかないと神経細胞の生存を永らえさせることはできない。
・今はいかにして早期に始めるのかということが問題。
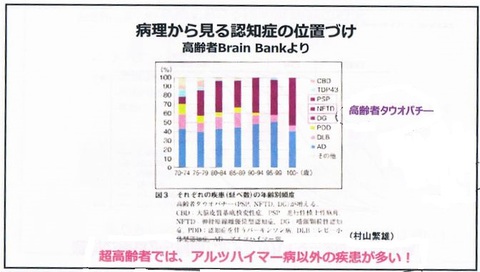
・これは超高齢者の脳を見た論文、70代、80代、100代と、紫色がどんどん増える。高齢者の脳を連続的に剖検、病理学的な検索を行ったもの。
・高齢者の脳はアルツハイマー病(注:グラフの水色)は一定数多い。しかし、この紫色が100歳以上では半分以上。つまり超高齢者の認知症はアルツハイマー病以外の疾患で引き起こされることが明らかになった。
これらはまとめて「高齢者タウオパチー」と呼ばれる。神経原線維変化が集まってできた病気で、アルツハイマー病とは全く違う病気と分かっている。
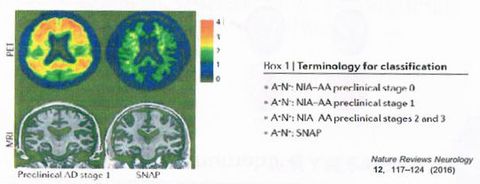
・これはアミロイドPETを示したもの。左側が老人斑がたまっていて、右側はたまっていない。こういうものをまとめてSNAP(Suspected non-amyloid pathophysiology)と呼ぶ。高齢者タウオパチーもSNAPの一部となる。現在はアルツハイマー病や老化についてこういう考えがコンセンサスになってきている。
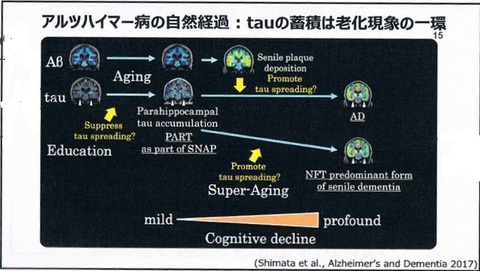
・神経原線維変化は老化と共に起きるもので、今の科学ではなかなか防ぎようがない。これは6歳の子どもでも1,2個あると言われ、老化と共にTauの沈着は起きる。
・アミロイドβの蓄積は起きる人と起きない人がいる。起きる人は無症状で脳にびっしりとたまる。この老人斑がどういうメカニズムか分からないが、TAUの、神経原線維変化の沈着を促す。そして老化によって広がっていたTAUがどんどん広がっていく。この最終形態がアルツハイマー病。
・老人斑がないとどうなるかというと、運よくあまり広がらない人もいれば、Tauだけたまり続け、100歳になる頃にはTauがびっしりとたまる。これが高齢者タウオパチー。
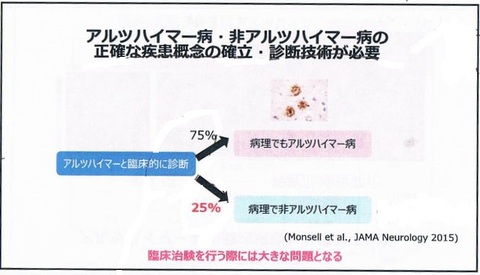
・今まで私達はPETの検査ができなかったので、全部アルツハイマー病と考えていた。ところが実際脳を見てみると、いろんな病気が混在していて、その中の大部分をアルツハイマー病が占めるのだが、そうじゃないものもたくさんある、ということが分かってきた。
・物忘れがあってアルツハイマー病と診断されていたケースが、病理を開けてみてみると25%、4分の1がアルツハイマー病じゃなかった。いわゆるSNAPのような病態だと分かってきた。
・今まではこれらを全部一緒に、アルツハイマー病としての臨床治験していた。アミロイドを減らせばいいとして、アミロイドをターゲットにした治験をしていた。しかし、全部一緒にすると当然アミロイドのない脳には全く効果がない。元々しっかりとした疾患概念、診断技術が確立していなければ治験が成功するはずがない。
・今はアルツハイマー病という患者にはPET検査、髄液検査が必要になってきている。薬物療法の限界という点からいえば、治験失敗の訳は、認知症発生時には取り返しのつかないぐらい多くの神経細胞が死んでいたということ。その時点で何か病態的なアプローチをしようと思っても、再生してこない神経が生まれ変わることはないので難しいということ。高齢者を中心にアルツハイマー病以外のSNAPという病態が意外に多かったということ。
・これからの治験は超早期からの介入の必要がある。それでも超早期というのはまだ診断も何もなされていない、症状も出ていない状況。それなら、一体誰に、どのような形で介入していくのかということが問題になる。病態を反映する正確な診断技術も必要になる。これまでのように認知症で物忘れがあったらアルツハイマー病として考えるのではなく、正確に診断していく必要がある。また抗アルツハイマー病治療薬が開発されて老人斑がなくなったとしても、タウオパチーが残る。これは老化と密接に関係している。神経細胞の老化そのものを防ぐことが本当に可能なのかどうかという問題が出てくる。
関連するロハス・メディカルの記事
特集 認知症を知る
①きほんのき(2012年6月号)
②アルツハイマー型(2012年7月号)
③レビー小体型(2012年8月号)
④脳血管性(2012年9月号)
⑤その他の原因(2012年10月号)